Insuline
L’insuline est une hormone peptidique produite par les cellules bêta des îlots de Langerhans dans le pancréas. Elle joue un rôle central dans la régulation du métabolisme des glucides, des lipides, et des protéines, en facilitant l’absorption du glucose par les cellules et en maintenant l’homéostasie de la glycémie (taux de sucre dans le sang). L’insuline est essentielle pour le stockage de l’énergie et la gestion des nutriments après un repas.
Synthèse et libération de l’insuline :
- Production dans le pancréas :
- L’insuline est synthétisée sous forme de précurseur appelé préproinsuline. Après une série de modifications, elle devient proinsuline, qui est ensuite transformée en insuline active et en peptide C dans les cellules bêta du pancréas.
- L’insuline et le peptide C sont stockés dans des vésicules sécrétoires, prêts à être libérés dans le sang lorsque la glycémie augmente.
- Stimulus pour la libération :
- La libération d’insuline est principalement déclenchée par une augmentation de la glycémie après un repas. Lorsque le glucose entre dans les cellules bêta via les transporteurs GLUT2, cela stimule la production d’ATP, qui entraîne la fermeture des canaux potassiques sensibles à l’ATP et l’ouverture des canaux calciques. Cela provoque une entrée de calcium dans la cellule et déclenche la libération d’insuline par exocytose.
- D’autres stimuli incluent les acides aminés, les acides gras et certaines hormones gastro-intestinales (comme l’incrétine, libérée après un repas).
Rôles et fonctions de l’insuline :
- Régulation de la glycémie :
- L’insuline est la principale hormone hypoglycémiante du corps. Après un repas, elle abaisse la glycémie en facilitant l’absorption du glucose dans les cellules, en particulier dans les muscles, le foie et les tissus adipeux.
- Elle stimule les transporteurs de glucose GLUT4, qui permettent au glucose d’entrer dans les cellules musculaires et adipocytaires.
- Stockage du glucose sous forme de glycogène (glycogenèse) :
- Dans le foie et les muscles, l’insuline stimule la conversion du glucose en glycogène (une forme de stockage du glucose) via un processus appelé glycogenèse.
- En même temps, l’insuline inhibe la glycogénolyse, qui est la dégradation du glycogène en glucose.
- Inhibition de la production de glucose par le foie (gluconéogenèse) :
- L’insuline inhibe la gluconéogenèse, le processus par lequel le foie produit du glucose à partir de précurseurs non glucidiques (comme les acides aminés ou le lactate). Cela contribue à réduire la production de glucose endogène et à maintenir des niveaux de glucose normaux.
- Stimulation du stockage des lipides (lipogenèse) :
- L’insuline favorise le stockage des acides gras sous forme de triglycérides dans les adipocytes. Elle active les enzymes qui stimulent la synthèse des acides gras (comme l’acétyl-CoA carboxylase) et inhibe la lipolyse, c’est-à-dire la dégradation des graisses.
- Promotion de la synthèse des protéines :
- L’insuline stimule l’absorption des acides aminés dans les cellules musculaires et favorise la synthèse des protéines en augmentant l’activité des enzymes impliquées dans la traduction et la transcription des protéines. Elle réduit également la protéolyse (la dégradation des protéines musculaires).
- Effets sur d’autres hormones :
- L’insuline a des effets antagonistes avec d’autres hormones comme le glucagon (qui stimule la libération de glucose par le foie) et l’adrénaline (qui favorise la dégradation des graisses et du glycogène). En inhibant ces hormones, l’insuline aide à maintenir l’équilibre métabolique en période d’abondance énergétique.
Pathologies liées à l’insuline :
- Diabète de type 1 :
- Le diabète de type 1 est une maladie auto-immune dans laquelle les cellules bêta du pancréas sont détruites par le système immunitaire, entraînant une production insuffisante ou nulle d’insuline. Cela empêche les cellules d’absorber le glucose, entraînant une hyperglycémie (taux de sucre élevé dans le sang).
- Les patients atteints de diabète de type 1 nécessitent des injections d’insuline pour réguler leur glycémie et prévenir les complications liées à l’hyperglycémie chronique.
- Diabète de type 2 :
- Le diabète de type 2 est caractérisé par une résistance à l’insuline : bien que le pancréas produise de l’insuline, les cellules du corps ne répondent pas correctement à cette hormone. Cela conduit à une hyperglycémie persistante.
- À long terme, les cellules bêta peuvent s’épuiser, réduisant la production d’insuline. Les facteurs de risque incluent l’obésité, la sédentarité, et des antécédents familiaux de diabète.
- Syndrome métabolique :
- Le syndrome métabolique est un ensemble de conditions qui inclut une résistance à l’insuline, une hyperglycémie, une hypertension, une obésité abdominale, et des troubles lipidiques (comme l’hypertriglycéridémie). Il augmente le risque de développer des maladies cardiovasculaires et le diabète de type 2.
- Hypoglycémie :
- Une hypoglycémie survient lorsque le taux de glucose dans le sang chute en dessous des niveaux normaux, souvent en raison d’une suralimentation en insuline (par exemple, chez les patients diabétiques sous insulinothérapie). Les symptômes incluent des tremblements, de la confusion, des palpitations, et dans les cas graves, une perte de conscience.
- Insulinome :
- Un insulinome est une tumeur rare des cellules bêta du pancréas qui entraîne une surproduction d’insuline. Cela peut provoquer des épisodes récurrents d’hypoglycémie.
Traitements et régulation de l’insuline :
- Insulinothérapie :
- Les patients atteints de diabète de type 1 ou de diabète de type 2 avancé nécessitent des injections d’insuline pour maintenir leur glycémie dans la normale. Différents types d’insuline sont disponibles, notamment l’insuline rapide (action rapide), l’insuline intermédiaire, et l’insuline lente (action prolongée).
- Médicaments sensibilisateurs à l’insuline :
- Dans le cas du diabète de type 2, des médicaments comme la metformine sont utilisés pour améliorer la sensibilité des cellules à l’insuline. D’autres médicaments, comme les inhibiteurs des DPP-4 et les agonistes des récepteurs GLP-1, augmentent la sécrétion d’insuline en réponse aux repas.
- Modifications du mode de vie :
- L’exercice physique et la perte de poids sont des stratégies clés pour améliorer la sensibilité à l’insuline et prévenir ou gérer le diabète de type 2.
- Une alimentation équilibrée, riche en fibres et faible en glucides raffinés, peut aider à stabiliser les niveaux d’insuline et de glucose dans le sang.
- Pompes à insuline :
- Les patients nécessitant un contrôle strict de leur glycémie peuvent utiliser des pompes à insuline, des dispositifs qui délivrent de l’insuline en continu ou en bolus (sur une courte durée) en fonction des besoins du patient.
Complications liées à l’insulinothérapie :
- Hypoglycémie :
- Un des risques majeurs de l’insulinothérapie est l’hypoglycémie, qui peut survenir lorsque trop d’insuline est administrée par rapport à l’apport en glucides. Il est important d’ajuster les doses en fonction de l’alimentation et de l’activité physique.
- Résistance à l’insuline :
- Dans certaines conditions, les patients peuvent développer une résistance à l’insuline en raison de facteurs comme l’obésité, un excès de graisses abdominales, ou des maladies inflammatoires chroniques. Cela entraîne un besoin accru en insuline pour maintenir la glycémie sous contrôle.
Effets de l’insuline sur d’autres systèmes :
- Effet sur le métabolisme lipidique :
- L’insuline inhibe la lipolyse (dégradation des graisses) dans les tissus adipeux, favorisant ainsi le stockage des graisses. Une résistance à l’insuline peut entraîner une dyslipidémie (anomalie des graisses sanguines) avec des taux élevés de triglycérides et une diminution du cholestérol HDL (le « bon cholestérol »).
- Effet sur les muscles :
- L’insuline est nécessaire pour favoriser l’entrée du glucose dans les cellules musculaires, où il est utilisé pour produire de l’énergie ou stocké sous forme de glycogène. Une carence en insuline entraîne une dégradation musculaire, car le corps cherche à mobiliser des acides aminés comme source d’énergie alternative.
- Effet sur les reins :
- Une glycémie élevée non contrôlée (comme dans le diabète) peut provoquer des lésions rénales au fil du temps, car les reins doivent travailler plus pour filtrer l’excès de glucose. Cette condition est appelée néphropathie diabétique.
Conclusion :
L’insuline est une hormone essentielle à la régulation du métabolisme du glucose, des lipides et des protéines. Elle permet aux cellules d’absorber le glucose pour produire de l’énergie ou le stocker pour un usage ultérieur. Les déséquilibres dans la production ou la fonction de l’insuline peuvent conduire à des conditions graves comme le diabète ou le syndrome métabolique. La gestion de l’insuline, par des modifications du mode de vie, des médicaments ou l’insulinothérapie, est cruciale pour maintenir une glycémie saine et prévenir les complications.
Insuline = Hormone de « mise en réserve »
| Sur les glucides : Rôle hypoglycémiant | Sur les lipides : Rôle de stockage | Sur les Protéines : Rôle anabolisant |
|---|---|---|
|
|
|
Insuline = Coupable n°1 du surpoids !
- Insuline = Prise de gras
- Activation de la lipogenèse
- Inhibition de la lipolyse
- Fringale liée à l’hypoglycémie réactionnelle induite
- Ce sont les aliments à charge glycémique élevée (et non les graisses) qui font grossir !
L’insuline
- Quantité insuline fonction de la VITESSE d’augmentation de la glycémie
- Aliments à CG élevé :
- Forte synthèse d’insuline → hypoglycémie réactionnelle
- Confusions, faiblesse, tremblements ou agitation, perte de concentration, sensation de faim, envie de sucre
- Forte synthèse d’insuline → hypoglycémie réactionnelle
- La personne aura tendance à se « resucrer ». Ceci entraine un véritable cercle vicieux
Insuline : mode de fonctionnement
- Pour faire rentrer le glucose dans la cellule, l’insuline doit
- Se fixer sur son récepteur
- Activer le récepteur
- Entraîner une translocation des transporteurs du glucose (Glut 4) au niveau de la membrane cellulaire
- Enfin, le glucose rentrera par le Glut 4 par effet d’osmose : dépendant du gradient de concentration du glucose entre extérieur et intérieur de la cellule
Conditions indispensables au fonctionnement du récepteur à l’insuline (IR)
| Membranes Fluides | Cofacteurs indispensable à l’activité des IR | ||
|---|---|---|---|
| Indispensable pour : | Magnésium | Zinc et chrome | |
|
|
|
|
| |||
Conditions indispensables au fonctionnement du récepteur à l’insuline (IR)
Absence d’inflammation
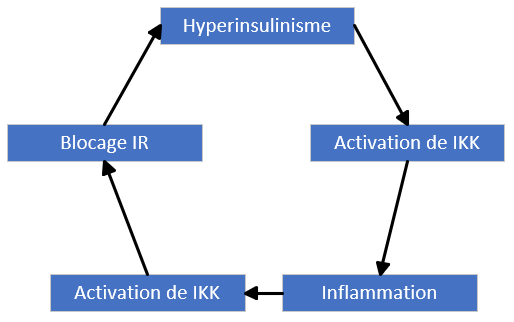
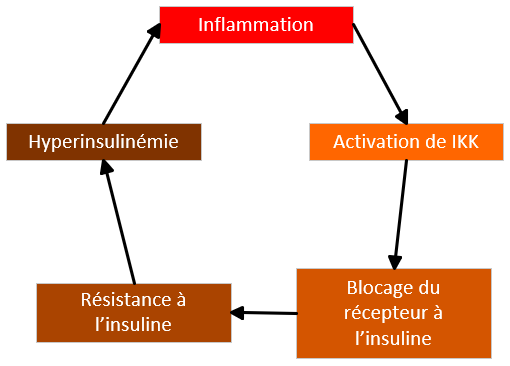
- Inflammation => activation de Kinase IKK => phosphorylation de IRS sur un mauvais site => blocage du IR
- => Résistance à l’insuline
- L’inflammation peut induire de l’hyperinsulinisme et une résistance à l’insuline
- ET l’hyperinsulinisme est également pro inflammatoire
- => cercle vicieux
Surcharge hépatique – Conséquences :
Variation de la sensibilité à l’insuline au cours de la journée
- IR plus sensibles le matin ++
- Ingestion de sucre le matin = hypoglycémie réactionnelle plus importante ++
- Au cours de la journée la sensibilité des IR ↘
Effondrement de l’insuline la nuit : indispensable à la lipolyse nocturne
- La lipolyse s’effectue la nuit
- GH (Hormone de croissance) ↗ Nuit : Renouvellement cellulaire beaucoup plus intense la nuit que le jour
- Nécessite accès à nos réserves de graisses
- Insuline doit être basse la nuit pour ne pas bloquer lipolyse
- Cortisol doit être bas la nuit (↕️lipolyse) et ↗ glycémie et ↗ insulinosensibilité
- Dans ce cas : LA LIPOLYSE NOCTURNE possible
Impact des aliments à CG élevés suivant le moment de la journée
- Matin :
- Aliments à CG élevée => hypoglycémie réactionnelle ++ => faim… => sucre… => hypoglycémie réactionnelle… => cercle vicieux => prise de poids
- Soir :
- Aliments à CG élevée => ↗ insuline nocturne => Inhibition lipolyse => Prise de poids
- Milieu d’après midi :
- Aliments à CG élevée : Moins d’impact
- Mais favoriser les CG bas pour un effet sérotoninergique durable